Nature封面重磅!劍橋大學團隊揭開老年癡呆背后的罪魁禍首
聽說過阿爾茨海默病嗎?沒有。老年癡呆癥總聽說過吧?
阿爾茨海默病,又稱老年癡呆癥,是一種發病進程緩慢、隨時間不斷惡化的神經退化性疾病。早期癥狀為喪失短期記憶(記不住最近發生的事),當疾病逐漸進展,后續可能出現語言障礙、定向障礙(容易迷路)、情緒不穩、無法自理以及許多行為異常問題。
目前,該病的發病機理仍不明確。科學界對阿爾茨海默病的病因提出了多種假設。近年來比較流行的兩種假設是Tau 蛋白異常和淀粉樣蛋白異常。
2020 年 1 月,發表在 Science Translational Medicine 上的一項研究顯示,對病理性 tau 蛋白纏結的腦成像能夠可靠地預測阿爾茨海默癥患者未來一年或更早出現腦萎縮的位置。相比之下,淀粉樣蛋白可能與阿爾茨海默病的關系不大。
這表明,tau 蛋白比淀粉樣蛋白更直接地導致阿爾茨海默癥的大腦退化。
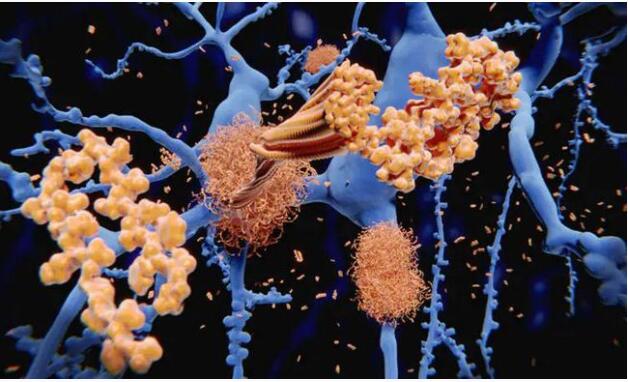
Tau 蛋白(Tau proteins)是一種微管相關蛋白,在中樞神經系統的神經元中含量非常豐富,而在其它細胞內比較少見。
tau 蛋白的主要功能之一是維持神經元軸突微管的穩定。 當 tau 蛋白有缺陷,不能起到穩定微管的作用時,就可能導致一系列神經系統病變,阿爾茨海默病正是其中的一種。
科學家將這類疾病統稱為 tauopathies,指的是由于大腦中 tau 蛋白結構異常而導致的神經退行性疾病,即「tau 蛋白病」。
顯然,tau 蛋白病并非只有一種,應該如何區分呢?既然這類疾病是由 tau 蛋白異常引起,那么,不同疾病之間的 tau 蛋白異常結構應該也是各有不同的。
實際上,通過冷凍電鏡,科學家們之前就發現阿爾茨海默病(Alzheimer's disease)、皮克病(Pick's disease)、慢性創傷性腦病(chronic traumatic encephalopathy,CTE)和皮質基底退化(corticobasal degeneration,CBD)的 tau 蛋白結構是不同的。
于是自然想到一種方法,通過 tau 蛋白折疊結構的不同來對 tau 蛋白病進行分類。
2021 年 9 月 29 日,英國劍橋大學 Sjors H. W. Scheres、Michel Goedert 等研究人員在 Nature 上發表了一篇論文,題為「Structure-based Classification of Tauopathies」,正式提出了這一方法。
https://www.nature.com/articles/s41586-021-03911-7
這篇文章登上了最近一期 Nature 的封面。
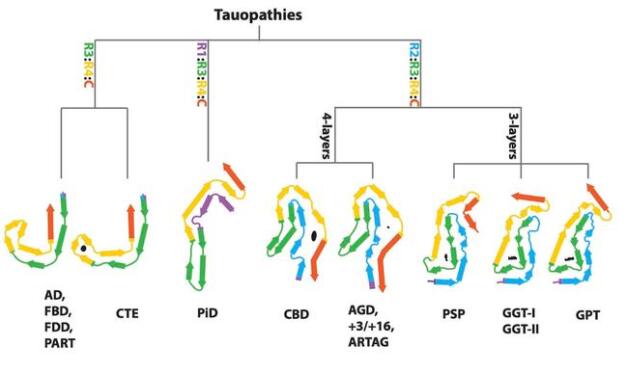
在本文中,研究人員提出了一種根據纖維折疊結構對 tauopathies 進行分級分類的辦法,這大大補充了臨床診斷和神經病理學的依據,并展現出可以識別新的 tauopathies 病例的潛力。
根據 tau 蛋白細絲折疊來分類 tau 蛋白病,圖片來自 MRC Laboratory of Molecular Biology
舉個例子吧。
上面提到過阿爾茲海默癥,其實,家族性英國癡呆(familial British dementia,FBD)和家族性丹麥癡呆(familial Danish dementia,FDD)病例 tau 絲的結構與阿爾茨海默病(AD)和原發性年齡相關 tau 蛋白病(primary age-related tauopathy,PART)病例中的結構相同。
再比如,進行性核上性麻痹(progressive supranuclear palsy,PSP)出現的頻率僅次于阿爾茲海默癥,也是一種常見的 tau 蛋白病。
這篇文章發現了進行性核上性麻痹(PSP)的 tau 絲結構是一個全新的三層折疊結構,而且球狀膠質陶氏病(globular glial tauopathy,GGT)的 tau 絲結構與進行性核上性麻痹(PSP)十分相似,只有尾端有所不同。
目前,科學家們正在努力尋找不同的 tau 蛋白褶皺形成的分子機制,不過結果現在仍是未知數。
Sjors H. W. Scheres 和 Michel Goedert 團隊也正在繼續研究此課題,如果有一天真的能破譯 tau 蛋白褶皺形成的分子機制,tau 蛋白病的診斷和治療將會迎來一個全新的時代。